心血管疾病始終高踞台灣國人十大死因的第二及第三位[11]。多數心血管疾病突發主要是動脈血管栓塞(arterial thrombosis),而其中血小板扮演關鍵角色。當動脈硬化斑塊破裂導致內皮下組織露出時,血小板會黏附其上,形成一易栓塞之介面。其後血栓形成,嚴重的時候便造成血管堵塞。
諸多臨床藥物試驗均顯示抗血小板藥物使用能有效降低各類心血管疾病患者的再發及死亡率。
所以今天的主角就是關於prasugrel與他相關的抗血小板藥物。
現今主要抗血小板的藥物有以下幾類
|
類別 |
藥物 |
|
Glycoprotein IIb/IIIa inhibitors |
Abciximab、Eptifibatide、Orbofiban、Roxifiban Sibrafiban、Tirofiban |
|
ADP receptor/P2Y12 inhibitors |
Thienopyridines:Clopidogrel、Prasugrel、Ticlopidine Nucleotide/nucleoside analogs:Cangrelor、Elinogrel、Ticagrelor |
|
Prostaglandin analogue (PGI2) |
Beraprost、Iloprost、Prostacyclin、Treprostinil |
|
COX inhibitors |
Acetylsalicylic acid/Aspirin、Aloxiprin、Carbasalate calcium、Indobufen、Triflusal |
|
Thromboxane inhibitors |
Thromboxane synthase inhibitors:Dipyridamole (+ aspirin) 、Picotamide、Terbogrel Receptor antagonists:Terbogrel、Terutroban |
|
Phosphodiesterase inhibitors |
Cilostazol、Dipyridamole、Triflusal |
|
PAR-1 antagonist |
Vorapaxar |
|
5-HT2A Antagonist |
Sarpogrelate、pizotifen、cyproheptadine |
|
其他 |
Cloricromen(semi-synthetic coumarin derivative)、Ditazole(thromboxane A2 inhibitor) |
儘管有這麼多種類的藥物,但是目前臨床上最廣泛使用的抗血小板藥物大約是阿司匹林(aspirin),保栓通(clopidogrel),及醣蛋白受器抑制劑Glycoprotein IIb-IIIa(GPIIb-IIIa)receptor inhibitor三類。
Aspirin主要機轉是經由抑制血小板內的cyclooxygenase I而抑制thromboxane A2合成,進而避免其與thromboxane prostanoid 受器結合,避免血小板的活化。此種抑制由於是不可逆性的,因此儘管aspirin在人體內的半衰期只有15-20分鐘,其藥效卻能持續7-10天,亦即要等血小板生命週期結束換一批新的才開始有凝血效果。Clopidogrel屬於thienopyridine類藥物,本身並無抗血小板作用,必須經由cytochrome P450代謝後才能產生具有抗血小板作用之代謝物,代謝物會與ADP的血小板受器P2Y12結合,於是抑制其所引發的血小板活化。此種抑制如同aspirin也屬不可逆性的。
GPIIb-IIIa受器抑制劑目前市面上可以使用的有abciximab、eptifibatide、tirofiban以及台灣沒有的Roxifiban和orbofiban五種。
血小板活化的最終反應會於血小板表面表現出大量的GPIIb-IIIa受器(約80,000個/每血小板),並藉此與其他血小板緊密結合。GPIIb-IIIa受器抑制劑能與GPIIb-IIIa(亦稱integrin αIIbβ3)受器結合而抑制其作用;亦由於其作用於血小板結合的關鍵受器,因此其抗血小板作用最強。
目前的抗血小板藥物確能有效減少動脈栓塞疾病發生,但亦有其缺點。如血小板抑制效果弱(如aspirin)、藥效起始需時較長(如clopidogrel)、不同人對同劑量藥物投與後產生的抗血小板作用差異頗大(如clopidogrel)、口服劑型少而且昂貴(如GPIIb-IIIa受器抑制劑)、無法將抗血栓作用與出血副作用分開等。
所以針對這些問題,加上現今科技對於血小板更為了解,新型態的抗血小板藥物相繼研發或接近臨床可使用階段,這些就是上述表格中的ADP P2Y12抑制劑(prasugrel, ticagrelor, cangrelor, elinogrel)、thrombin受器PAR1(Protease-activated receptors)拮抗劑(Vorapaxar/ Zontivity®)、Glycoprotein VI (GPVI), integrin α2β1, 5HT2A等受器抑制劑。
關於Prasugrel
開發與核准歷史
Prasugrel為日本第一三共和美國 Eli Lilly共同開發,並於2009年2月23日獲歐盟批准上市,應用於治療動脈粥樣硬化(atherosclerosis,AS)和急性冠狀動脈綜合症(ACS, Acute coronary syndrome)。
2009年2月, 歐盟批准prasugrel(Efient)用於預防已接受急診和將進行延遲經皮冠脈干預術的急性冠脈綜合徵患者的動脈粥樣硬化性血栓形成( atherothrombosis)事件。這是prasugrel在全球範圍內首次獲得批准。
簡要機轉
prasugrel為一新的口服有效thienopyridine 類藥物。與Clopidogrel一樣,prasugrel也是一個無活性的前體藥物,需經CYP 450酶系代謝轉化至活性代謝物後才能不可逆地抑制血小板上的P2Y12。
prasugrel的抗凝血效果比Clopidogrel較為快速,可以從藥動學性質改善得到解釋:prasugrel具有更高的前驅物至活性代謝物轉化率以及更高的生體可用率,所以onset更快並能降低個體間的療效差異,更大程度地降低主要缺血性心血管事件發生率。
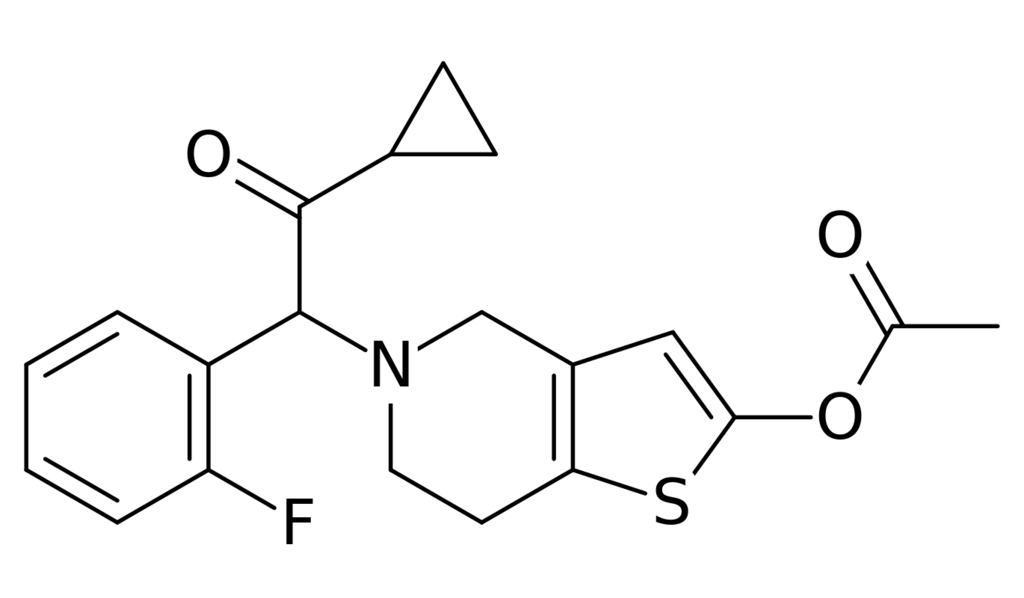
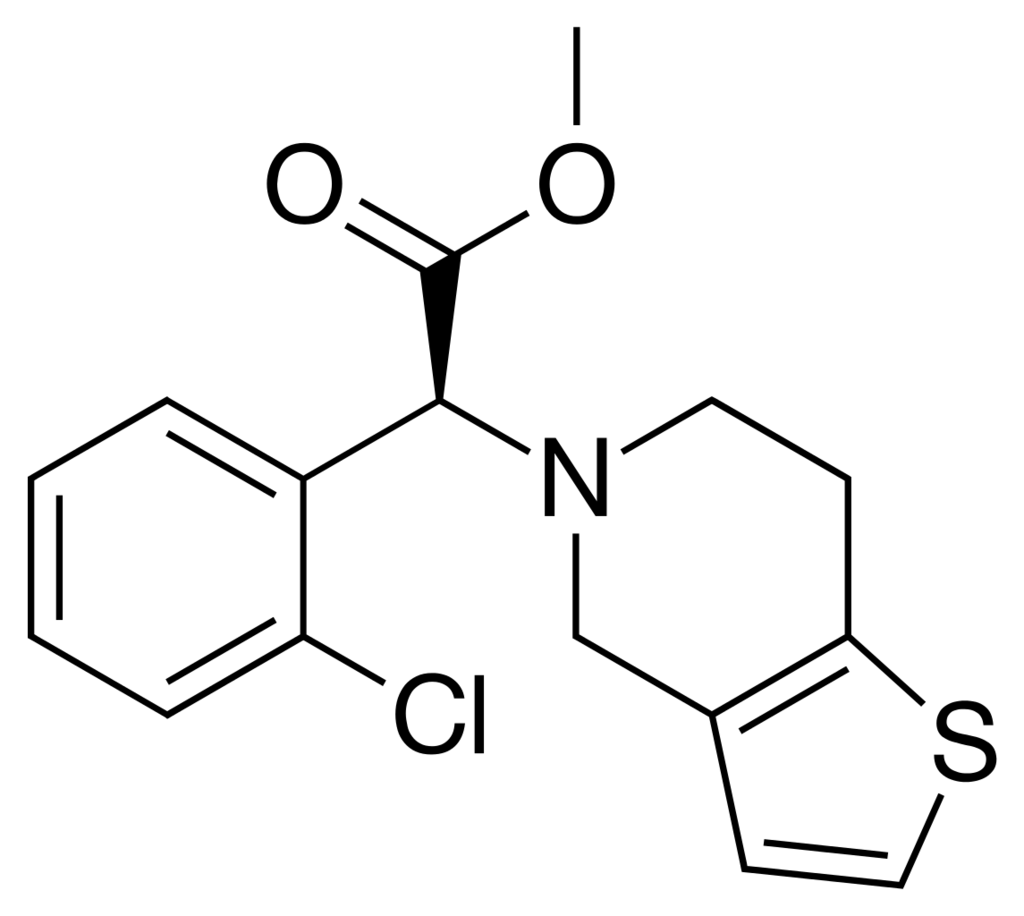
分子結構:
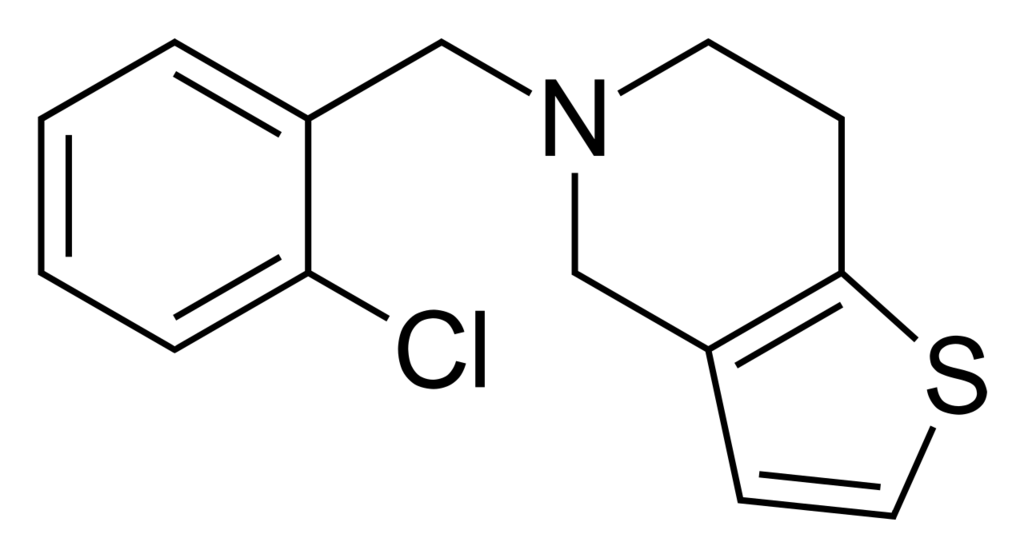
Prasugrel屬於thienopyridine類藥物,由主要的兩個分子官能基thiophene加上pyridine所構成。
與ticlopidide還有Clopidogrel的主要差異是ticlopidine還有clopidogrel的外接基團是以氯為主,而prasugrel是氟為主。
Ticlopidine
clopidogrel
Prasugrel 有兩個鏡像異構物,分別是:R-enantiomer (R- 96875) 與 S-enantiomer (R-96876)。
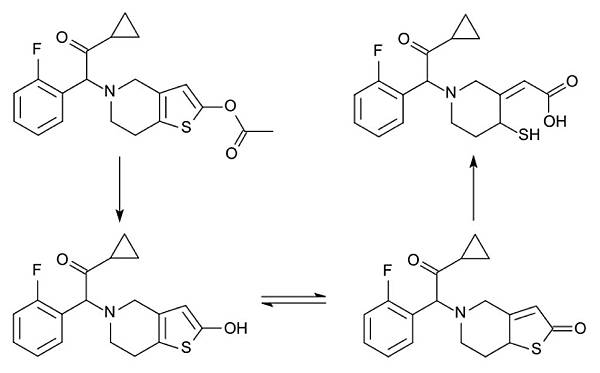
給予大鼠R-96875和R-96876(均為1和3mg / kg)分別在給藥後2和4小時劑量依賴性地抑制血小板聚集。在相同劑量下,R-96875和R-96876之間的功效沒有統計學上的顯著差異。給藥後4小時的ED 50值對於R-96875為1.4mg / kg,對於R-96876為1.3mg / kg。還在食蟹猴中檢查了使用富含血小板的血漿重複施用R-96875和R-96876(均為0.3mg / kg /天,口服)3天對ADP誘導的血小板聚集的影響。兩種處理之間的洗脫期被認為是可接受的。兩種異構體在第3天引起血小板聚集的抑制,並且這種效果在各組之間幾乎相等。在任何時候R-96875和R-96876之間的功效沒有統計學上的顯著差異。這些結果表明口服prasugrel的光學異構體R-96875和R-96876對大鼠和食蟹猴中的血小板聚集具有相似程度的離體作用。
活性代謝物R-138727(上圖右上角)具有兩個手性中心,產生四種對映體。代謝物R-138727具有有效和選擇性的P2Y12拮抗活性。 R-138727的兩種最有效的對映體R-125690和R-125689分別比對映體R-125687和R-125688的效力高約100倍和10倍。兩種最有效的對映體包括大鼠和人體中的大部分循環R-138727。
第I/II/III期臨床實驗資訊
Ⅰ期(節錄)
68名健康志願者分2階段交叉口服prasugrel60 mg負荷+維持量10 mg·d-1與Clopidogrel300 mg負荷+維持量75 mg·d-1,prasugrel組抑制血小板聚集作用顯著較Clopidogrel組強且快(IPA為78.8% vs 35%,P< 0.001),前者15 min即可出現顯著的血小板抑製作用,60 min內出現最強的抑製作用。在健康志願者及冠心病(CAD)患者中,prasugrel無效率均較Clopidogrel低。以IPA≤ 20%作為藥物抵抗標準,口服prasugrel60 mg與Clopidogrel300 mg負荷量24 h時,藥物抵抗發生率prasugrel為0,而Clopidogrel為42%。由於prasugrel活性代謝產物的體外半數最大血小板抑制濃度(IC50)1.8μmol·L-1與Clopidogrel2.4μmol·L-1相近,所以兩者作用差異較大的原因主要是Clopidogrel在體內產生的活性代謝產物較少,而非由於活性代謝產物與ADP受體P2Y12的結合異常。
Ⅱ期(節錄)
JUMBO-TIMI 26研究將900例擇期經皮冠脈介入(PCI)或急症PCI的CAD患者隨機分成4組,即prasugrel40 mg負荷+維持量7.5 mg·d-1、prasugrel60 mg負荷+維持量10 mg·d-1、prasugrel60 mg負荷+維持量15 mg·d-1、Clopidogrel300 mg負荷+維持量75 mg·d-1組,共服用30 d,研究終點為發生嚴重或輕度出血事件。結果prasugrel組的出血事件發生率較Clopidogrel組高,但差異無統計學意義(1.7% vs1.2%,P= 0.59)。儘管該研究設計為臨床安全性研究,未對臨床療效的統計效能進行檢驗,但仍顯示prasugrel組的嚴重心臟不良事件發生率較Clopidogrel組有降低趨勢,尤其是靶血管血栓形成發生率較低,且差異有統計學意義(P< 0.05)。[1]
Ⅲ期(節錄)
TRITON-TIMI 38研究為隨機雙盲研究,主要研究終點(心血管原性死亡、非致死性心梗、非致死性卒中)事件發生率prasugrel組顯著低於Clopidogrel組[9.9%vs 12.1%,風險比(HR)0.81,95%CI 0.73~0.90,P< 0.001]],其療效優勢開始於治療後第3天(4.7% vs 5.6%,HR 0.82,95%CI 0.71~ 0.96,P=0.01),並持續至整個隨訪期。支架內血栓形成發生率顯著較低(1.1% vs 2.4%,HR 0.48,95%CI0.36~0.64,P< 0.001)。但TIMI嚴重或輕度出血事件發生率顯著較高(5.0% vs 3.8%,HR 1.31,95%CI 1.11~1.56,P= 0.002),其中TIMI嚴重出血事件發生率顯著較高(2.4% vs 1.8%,HR 1.32,95%CI 1.03~1.68,P= 0.03),致死性出血事件發生率也顯著較高(0.4% vs 0.1%,P= 0.002)。儘管prasugrel組增加了出血事件,但聯合終點事件(死亡、非致死性心梗、非致死性卒中、TIMI嚴重出血)發生率仍低於Clopidogrel組(12.2% vs 13.9%,HR0.87,95%CI 0.79~0.95,P= 0.004),臨床淨獲益有益於prasugrel組。糖尿病患者主要終點事件相對危險降低了30%,而嚴重出血無差異。事後亞組分析顯示既往卒中或TIA史、75歲以上老年患者、體質量低於60 kg的低體質量患者prasugrel治療無淨獲益,既往卒中或TIA史患者prasugrel組的聯合終點事件發生率甚至顯著高於Clopidogrel組(23.0% vs16.0%,HR 1.54,95%CI 1.02~2.32,P= 0.04)。
其他臨床研究
ACCOAST 試驗
prasufrel在針對 NSTEMI 病患的國外臨床試驗中,相較於 PCI 時直接給予標準起始劑量 60 mg,若將起始劑量分別在冠狀動脈攝影約 4 小時前給予起 始劑量 30 mg 並在 PCI 時給予另外起始劑量 30 mg,會造成術 間嚴重出血的風險升高,而無實質效益。
RAPID(Prasugrel與Ticagrelor比較)
對於RAPID(Rapid Activity of Platelet Inhibitor Drugs)試驗,Careggi university hospital(位於意大利Firenze)的Guido Parodi及同事隨機挑選了50位實施直接經皮冠狀動脈介入術的ST段抬高心肌梗死患者,對他們進行比伐盧定單藥治療,負荷劑量為prasugrel 60 mg (n = 25) 或ticagrelor 180 mg (n = 25)。 殘餘血小板活動使用VerifyNow P2Y12化驗(由位於加州聖地亞哥的愛科美思公司完成)評估,分別為基線、2、4、8與12小時。
2小時後,整體PRU值範圍為2至398,中間值為242。prasugrel與ticagrelor的PRU值沒有太大差異(217對比275; P = 0.207),都符合非劣效性標準。 prasugrel在8小時後的血小板抑制效果略遜於ticagrelor(P < 0.01)。 此外,讓患者從高血小板反應範圍(PRU ≤ 240)轉換仍需prasugrel3 ± 2 小時及ticagrelor5 ± 4 小時。表示prasugrel在3至5小時後有效抑制血小板
而嗎啡的使用(OR 5.29;95% CI 1.44-19.49;P = 0.012)與基線PRU值(OR 1.014;95% CI 1.00-1.03;P = 0.046)都為高血小板反應性的獨立預測因子。
兩項試驗之間的事件率沒有差異,但使用ticagrelor治療則報告了更高的呼吸困難與對比劑腎病比率。 此外,2位使用ticagrelor的病人因頑固性心力衰竭死亡,1位prasugrel組具有高血小板反應性的病人在直接經皮冠狀動脈介入術後的3小時後出現支架血栓。
PROMETHEUS
研究數據表明,在全美醫學科學研究中心的急性冠脈綜合徵(ACS)患者中,Prasugrel使用者與Clopidogrel使用者的臨床表現存在很大差異。
Usman Baber(Icahn School of Medicine at Mount Sinai)在心血管造影與介入治療協會科學會議上報告了其研究指出Prasugrel使用者的缺血與出血事件風險負擔低於Clopidogrel使用者。
Baber等人於2010年1月至2013年6月在8家美國醫學科學研究中心進行了回顧性隊列研究,共納入19914例植入支架的PCI患者。研究者通過各個醫療中心的數據庫收集了患者的基線、臨床手術及預後數據,並根據患者PCI時使用Clopidogrel或Prasugrel對其進行分類。
20%患者(n=4058)在行PCI時接受Prasugrel治療,其餘接受Clopidogrel治療。Clopidogrel組患者的主要有效終點(PCI後90天主要不良心臟事件)發生率為9.6%,Prasugrel組為5.7%(P < .001)。這意味著Prasugrel可使整體MACE相對風險降低42%。校正基線差異後,相對風險降低變為11%,無明顯意義。
經過校正,兩組間的主要安全終點(需住院的術後或臨床明顯出血)已不存在顯著差異(3.8% vs. 4%;P= 0.52)。
儘管研究顯示Prasugrel可降低缺血性不良事件的發生率,但經校正基線差異後,獲益程度減弱,且不再具有統計學意義。缺乏校正Prasugrel出血差異可能反映出對低危出血患者的選擇性。結果表明Prasugrel比Clopidogrel更適用於低危PCI患者。與Clopidogrel使用者相比,Prasugrel使用者更為年輕,多為男性,且腎功能損害與貧血者較少。但Prasugrel使用者更易表現出STEMI,且需要更長的支架治療過程。
Prasugrel使用者發生缺血及出血事件的風險因素負擔明顯較低。重新校正Prasugrel的真實使用情況可以更好的評估患者缺血風險,從而產生更明顯的治療獲益,這是個值得前瞻性評估的假設。[4]
現階段針對抗血小板聚集藥物的主要臨床試驗包括TRITON-TIMI 38, PLATO和CHAMPION PHOENIX試驗,後者促使美國在2015年6月通過了Kengreal(cangrelor) 的上市。然而,這些研究並無對比意義。
在TRITON-TIMI 38和 PLATO研究中,入組患者均為ACS患者,而CHAMPION-PHEONIX研究中約44%為ACS患者。在TRITON-TIMI 38和 PLATO研究中,大多數患者應用血小板表面糖蛋白IIb/IIIa受體拮抗劑,然而在CHAMPION-PHEONIX研究中該比例為0。幾個試驗的終點試驗也不相同。[6]
不過,當prasugrel還在審查時,美國致力於醫藥議題之非營利團體公共市民(Public Citizen)即寄信給美國FDA,對於用來支持prasugrel上市的臨床試驗TRITON-TIMI 38(Therapeutic Outcomes by Optimizing Platelet Inhibition with Prasugrel- Thrombolysis in Myocardial Infarction 38)數據提出疑慮,認為尚無法證明該藥物較clopidogrel有效與安全性,呼籲美國FDA應終止此藥物的審查。此封信並由prasugrel藥物專利申請權人Victor Serebruany博士聯合署名。
根據美國公共市民的信件內容,指稱TRITON-TIMI 38最主要的問題在試驗中prasugrel的劑量設計不當。試驗中prasugrel採用起始60毫克、以及每日10毫克的劑量,與對照之clopidogrel起始300毫克、每日75毫克相較之下,強度高了約2.5倍。就像是一場不公平的競爭。
此外,2010年,Serebruany博士亦於美國心臟病學期刊發表其對於TRITON-TIMI 38試驗數據的疑慮。Serebruany博士認為,美國FDA雖將試驗數據公開,然而面對這900多頁的資料,對於在臨床執業的心臟科醫師來說,想要從中獲得什麼有參考價值的資訊,都是十分困難的;而其中關於死亡率數據的部分,其實是值得關注的。整體觀之,prasugrel看似有較少的心血管死亡事件(133 vs 150),但卻有較多的出血死亡事件(21 vs 5)。另外,根據試驗中呈現的詳細死亡分布資訊,prasugrel治療對於STEMI病人有相對低的死亡率,且該優勢能穩定維持將近14個月;然而,對於不穩定型心絞痛(UA)或NSTEMI的病人,prasugrel在死亡率控制的表現,其實是略遜於clopidogrel[4]。

事實上,自2009年prasugrel核准之後,以prasugrel與clopidogrel比較的試驗與分析研究此起彼落,正反立場各執一詞。例如,同樣是以TRITON-TIMI 38試驗數據進行分析,也有主張prasugrel對不穩定型心絞痛(UA)或NSTEMI在降低主療效指標(primary end point, 包括心血管因素死亡、心肌梗塞死亡、中風死亡)的部分是優於clopidogrel的[7]。
2017年12月國際心臟病學期刊一篇世代研究指出,認為臨床使用prasugrel或clopidogrel治療,對於病人2年QALYs(quality adjusted life years, 品質調整存活年)無顯著差異,主張clopidogrel為經濟上較優勢的治療策略[8];隔年1月該期刊則有致編輯信提出反對立場,認為綜觀現有證據,prasugrel才是更符合成本效益的治療選擇[9]。
2012年,一項由prasugrel廠商(Eli Lilly & Daiichi Sankyo)贊助的、大型臨床隨機試驗TRILOGY ACS,於新英格蘭醫學期刊發表了與TRITON-TIMI 38不同結論的研究結果。該試驗包含7,243名未滿75歲有在服用aspirin的病人,試驗維期30個月,比較prasugrel 10mg/day與clopidogrel 75mg/day。後續並有以2,083位75歲以上病人進行研究,prasugrel則減至5 mg/day。此試驗研究團隊的結論認為:對於不穩定型心絞痛(UA)或NSTEMI的病人,prasugrel在降低主要療效指標(心血管因素死亡、心肌梗塞死亡、中風死亡)發生頻率的能力,並未與clopidogrel有顯著差異;在出血風險亦同。與前述Serebruany博士所提出的結論相近。
2013年,同樣由prasugrel廠商贊助、並以TRILOGY ACS進行的分析研究進一步指出,對於曾進行心臟血管成形術(angioplasty)的病人,prasugrel比clopidogrel有較少的心血管因素死亡、心肌梗塞死亡、中風死亡[10]。這篇研究刊登於知名的Lancet期刊,可以從中感覺廠商持續投注相當的成本在prasugrel之研究及推廣。
隨著越來越多的試驗與臨床數據累積,或許將逐步拼湊出prasugrel更貼近真實臨床的療效及安全性。但如同Serebruany博士所傳達的,重點其實是當初用來核准prasugrel上市的試驗證據受到操弄,美國FDA似有選擇性地呈現有利於核准該藥物的資料。這些不透明的過程,使TRITON-TIMI 38試驗數據滋生更多混淆,進而影響對prasugrel的評估與使用[2]。
相較於美國FDA於黑框警語中所列之禁忌症 – 曾有短暫性腦缺血(俗稱小中風)、中風病史的病人,台灣仿單則是列於「注意事項」,僅要求醫師謹慎使用。而在年長者用藥的部分,台灣仿單僅有以「老年病患通常生理功能較為下降,請謹慎使用,並觀察他們的狀況」形式上的提醒。不過,在有關手術前停止使用prasugrel的日數建議,台灣仿單則建議至少於14天前。
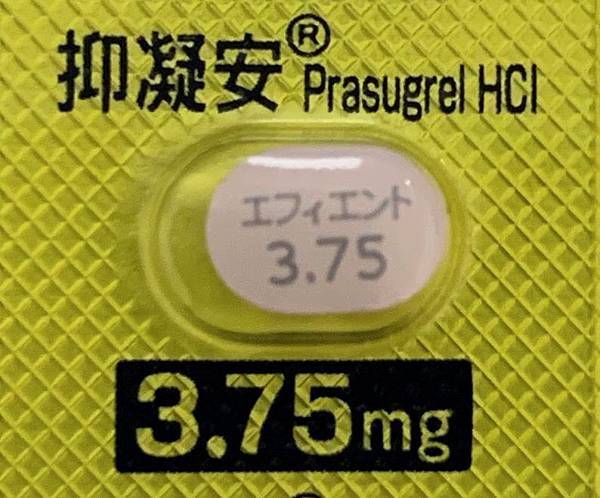
Prasugrel在台灣目前僅有原廠藥抑凝安®(Efient®)
仿單中主要以日本臨床試驗數據為參考訂定劑量,相較於美國FDA核准的起始60毫克/每日10毫克,台灣仿單建議為起始20毫克/每日3.75毫克。在其他出血危險因子的部分,台灣以50公斤為體重偏低之分野。
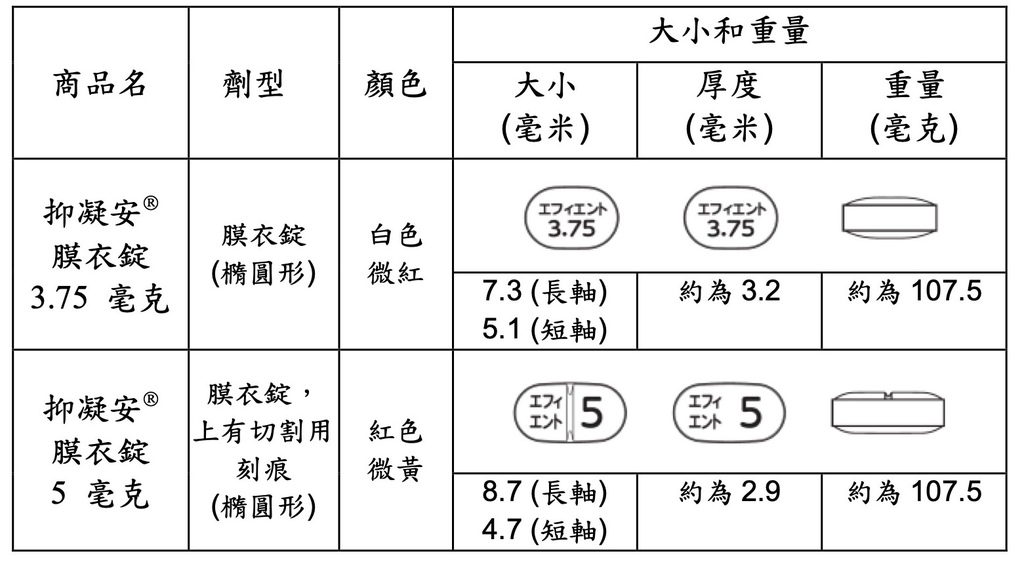
錠劑特寫:
規格文獻
相關賦形劑:
Lactose hydrate, microcrystalline cellulose, low substituted hydroxypropylcellulose, hydroxypropylcellulose, magnesium stearate, hypromellose, titanium oxide, talc, and red ferric oxide
用法與用量:
1.Efient的起始劑量為單次使用 20mg 口服劑量,隨後的維持劑量則採用每日一次 3.75mg 口服劑量。
Efient應合併 aspirin 使用(81 - 100 mg/天,起始劑量最多為 324 mg)。
2. 植入支架的病患使用 Efient之前,請先詳閱支架說明書。
3. 在進行 PCI 之前,已經接受 Efient 3.75 mg 劑量約 5 天的病患,不需要使用起始劑量(即治療第一天的起始劑量 20mg)。(Efient所引發的血小板凝集抑制作用,預計會在 5 天內達到穩定狀態。)
4. 不建議於空腹情況下使用 Efient (使用起始劑量時除外)。
手術前停用時間
建議臨床醫師在術前至少14天停止使用Efient
藥物動力學:
吸收和分布
prasugrel口服後在腸道迅速完全吸收,其代謝物R-138727的吸收與分布並無組織選擇性。動物試驗表明,小鼠和犬口服prasugrel後,均在1h內達血藥峰濃度(Cmax),大鼠口服5 mg/kg 的prasugrel後在0.83 h左右達Cmax 2.68μg Eq/mL,半衰期為23 h, AUC可達到36.2~47.1μg Eq/mL。[3]
代謝和排泄
prasugrel的代謝首先在腸壁、肝臟和血液內經酯酶水解變成硫代內酯類非活性代謝物(R-95913),然後經過細胞色素P450酶系統(主要是CYP3A和CYP2B6同工酶)的氧化作用變成活性代謝物R-138727,然後與血小板P2Y12-ADP結合,發揮抗血小板聚集作用。
經由胃部灌入給予大鼠放射性元素標記的prasugrel 1h,其組織和排泄物中均可檢測到較強的放射活性,經膽汁排泄的放射性標記物達90.1 %,但62.4%被重吸收;隨尿液和糞便排泄的放射性物質含量分別是20.2%和78.7%,提示,prasugrel及其代謝物主要經膽汁隨糞便排泄。
相關交互作用:
- 主要的交互作用是在於所有的抗凝血劑,均會有增加出血的可能。
- 在statin類的藥物並沒有顯著交互作用。
- 制酸劑如H2 blocker還有PPI雖然對於AUC沒有影響,但是會減少最大濃度約14-29%,所以在第三期試驗中顯示盡量避免與制酸劑同時服用。
- 關於同時服用CYP3A的抑制劑時,Ketoconazole會降低最大濃度約34-46%,但是其他的CYP3A抑制劑例如azol 類的antifungals、HIV protease inhibitors、clarithromycin、telithromycin、verapamil、diltiazem、ndinavir、ciprofloxacin、與葡萄柚汁對於prasugrel的藥物動力學並沒有顯著影響。
- 對於acute coronary syndrome的患者同時使用嗎啡類藥物的時候會減緩prasugrel以及其代謝物的效果,可能跟腸道的抑制有關,所以同時使用的時候會建議prasugrel使用非腸胃道的給藥方式。
Reference:
- http://www.timi.org/index.php?page=jumbo-timi-26
- De Servi S, et al. (2014).Clinical outcomes for prasugrel versus clopidogrel in patients with unstable angina or non-ST-elevation myocardial infarction: an analysis from the TRITON-TIMI 38 trial. Eur Heart J Acute Cardiovasc Care. 3(4):363-72.
- ASSESSMENT REPORT FOR Efient Procedure No. EMEA/H/C/000984
- Serebruany VL (2010). Mortality in the TRITON Trial: Update from the FDA Prasugrel Action Package. The American Journal of Cardiology 105(9):1356–7.
- Baber U, et al. Late-Breaking Clinical Trials. Presented at: Society for Cardiovascular Angiography and Interventions Scientific Sessions; May 6-9, 2015; San Diego.
- https://www.medscape.com/viewcollection/33493
- Wein B, et al. (2017). Prasugrel vs. clopidogrel in contemporary Western European patients with acute coronary syndromes receiving drug-eluting stents: Comparative cost-effectiveness analysis from the BASKET-PROVE cohorts. Int J Cardiol. 248:20-7.
- Spartalis M, et al. (2018). Cost-effectiveness of prasugrel versus clopidogrel in acute coronary syndrome patients undergoing percutaneous coronary intervention. Int J Cardiol. 251:32.
- Roe MT, et al. (2012). Prasugrel versus clopidogrel for acute coronary syndromes without revascularization. N Engl J Med. 367(14):1297-309.
- Wiviott SD, et al. (2013). Prasugrel versus clopidogrel for patients with unstable angina or non-ST-segment elevation myocardial infarction with or without angiography: a secondary, prespecified analysis of the TRILOGY ACS trial. Lancet. 382(9892):605-13.
- https://www.mohw.gov.tw/cp-16-48057-1.html





 留言列表
留言列表
 線上藥物查詢
線上藥物查詢 